Hukum Perbandingan Tetap atau yang dikenal juga sebagai Hukum Proust adalah salah satu konsep penting dalam ilmu kimia. Hukum ini pertama kali diperkenalkan oleh seorang ahli kimia asal Prancis bernama Joseph Louis Proust pada abad ke-18. Hukum Proust menyatakan bahwa dalam senyawa tertentu, unsur-unsur pembentuknya selalu terkandung dalam perbandingan tetap beratnya.
Hukum Proust atau Hukum Perbandingan Tetap Menyatakan Bahwa
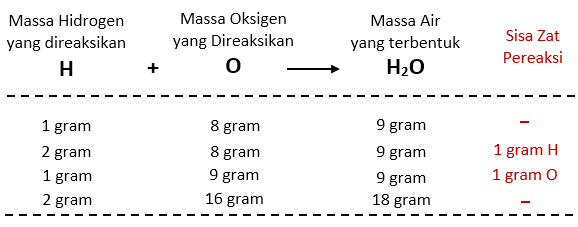
Hukum Perbandingan Tetap atau Hukum Proust menyatakan bahwa dalam senyawa kimia tertentu, elemen-elemen pembentuknya selalu terkandung dalam perbandingan tetap beratnya. Dengan kata lain, perbandingan berat antara unsur-unsur pembentuk senyawa akan selalu konstan di setiap senyawa yang sama. Misalnya, jika kita mempelajari senyawa air (H2O), kita tahu bahwa perbandingan berat antara hidrogen (H) dan oksigen (O) selalu 2:1. Ini berarti bahwa setiap molekul air terdiri dari dua atom hidrogen dan satu atom oksigen.
Apa itu Hukum Proust?
Hukum Proust, juga dikenal sebagai Hukum Perbandingan Tetap, adalah prinsip fundamental dalam kimia yang menyatakan bahwa dalam senyawa kimia tertentu, unsur-unsur pembentuknya selalu terkandung dalam perbandingan tetap beratnya. Hukum ini ditemukan oleh Joseph Louis Proust pada abad ke-18.
Siapa Joseph Louis Proust?
Joseph Louis Proust adalah seorang ahli kimia Prancis yang lahir pada tahun 1754 dan meninggal pada tahun 1826. Ia dikenal sebagai penemu Hukum Proust atau Hukum Perbandingan Tetap dalam kimia. Proust juga melakukan penelitian tentang hubungan antara komposisi senyawa kimia dan sifat-sifatnya.
Hukum Perbandingan Tetap dalam Prakteknya
Untuk lebih memahami Hukum Proust, mari kita lihat contoh penggunaannya dalam kehidupan sehari-hari. Salah satu contoh yang paling umum adalah perbandingan berat antara oksigen dan hidrogen dalam air. Air terdiri dari dua atom hidrogen (H) dan satu atom oksigen (O), sehingga perbandingan berat antara keduanya adalah 2:1. Artinya, setiap dua bagian hidrogen dihubungkan dengan satu bagian oksigen dalam air. Hal ini berarti bahwa dalam setiap molekul air, ada dua kali berat hidrogen dibandingkan dengan berat oksigen.
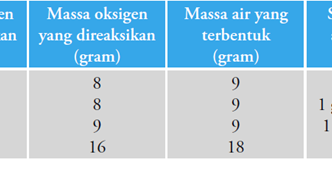
Jadi, bagaimana Hukum Proust ini diterapkan dalam senyawa lain selain air? Jika kita mengamati senyawa seperti amonia (NH3), kita akan melihat bahwa perbandingan berat antara hidrogen dan nitrogen adalah 3:1. Ini berarti bahwa setiap molekul amonia terdiri dari tiga atom hidrogen dan satu atom nitrogen.
Kapan Hukum Proust Ditemukan?
Hukum Proust ditemukan oleh Joseph Louis Proust pada tahun 1801. Pada saat itu, Proust sedang melakukan penelitian tentang komposisi senyawa kimia. Ia menemukan bahwa perbandingan berat antara unsur-unsur pembentuk senyawa selalu tetap, tidak peduli dari mana senyawa itu berasal.
Dimana Hukum Proust Berlaku?
Hukum Proust berlaku di semua senyawa kimia. Ini berarti bahwa dalam setiap senyawa kimia, perbandingan berat antara unsur-unsur pembentuknya akan selalu tetap. Baik itu senyawa anorganik maupun senyawa organik, hukum ini tetap berlaku.

Bagaimana Hukum Proust Bekerja?
Hukum Proust bekerja berdasarkan prinsip bahwa dalam senyawa kimia tertentu, unsur-unsur pembentuknya akan terkandung dalam perbandingan tetap beratnya. Ini berarti bahwa jika kita memiliki suatu senyawa dan kita tahu komposisinya, kita dapat menggunakan Hukum Proust untuk memprediksi perbandingan berat antara unsur-unsur pembentuknya.
Cara Menghitung Perbandingan Berat
Untuk menghitung perbandingan berat antara unsur-unsur pembentuk senyawa, kita perlu mengetahui bobot atom masing-masing unsur. Setelah itu, kita dapat menggunakan Hukum Proust untuk menghitung perbandingan beratnya.
Contoh Soal:
Jika suatu senyawa dibentuk oleh 16 gram karbon (C) dan 32 gram oksigen (O), hitunglah perbandingan berat antara kedua unsur ini dalam senyawa tersebut.
Jawab:
Untuk menghitung perbandingan berat antara karbon dan oksigen, kita harus menghitung jumlah mol masing-masing unsur terlebih dahulu. Kita dapat menggunakan rumus:
Jumlah mol = jumlah massa (dalam gram) / massa molar unsur
Massa molar karbon (C) = 12 gram/mol
Jumlah mol karbon = 16 gram / 12 gram/mol = 1.33 mol
Massa molar oksigen (O) = 16 gram/mol
Jumlah mol oksigen = 32 gram / 16 gram/mol = 2 mol
Jadi, perbandingan berat antara karbon dan oksigen dalam senyawa tersebut adalah 1.33:2, yang dapat disederhanakan menjadi 2:3.
Kesimpulan
Hukum Perbandingan Tetap atau Hukum Proust adalah prinsip dalam kimia yang menyatakan bahwa dalam senyawa tertentu, unsur-unsur pembentuknya selalu terkandung dalam perbandingan tetap beratnya. Hukum ini ditemukan oleh Joseph Louis Proust pada tahun 1801 dan berlaku untuk semua senyawa kimia. Hukum Proust bekerja berdasarkan prinsip bahwa dalam senyawa kimia, perbandingan berat antara unsur-unsur pembentuknya akan selalu tetap. Hukum ini penting dalam memahami komposisi dan sifat-sifat senyawa kimia. Dengan menggunakan Hukum Proust, kita dapat memprediksi perbandingan berat antara unsur-unsur pembentuk senyawa dan merancang percobaan untuk menguji kebenarannya.