
Hukum Proust Atau Hukum Perbandingan Tetap Menyatakan Bahwa
Hukum Proust, juga dikenal sebagai Hukum Perbandingan Tetap, adalah salah satu konsep yang sangat penting dalam ilmu kimia. Hukum ini menyatakan bahwa ketika dua elemen atau senyawa bergabung untuk membentuk suatu senyawa, massa relatif dari setiap elemen atau senyawa akan selalu berada pada perbandingan tetap.

Hukum Perbandingan Tetap (Proust) – Konsep, Bunyi dan Contoh Soal
Hukum Perbandingan Tetap, atau yang lebih dikenal sebagai Hukum Proust, merupakan salah satu dari teori-teori dasar dalam kimia. Hukum ini menyatakan bahwa ketika dua unsur atau senyawa bereaksi untuk membentuk senyawa tertentu, massa dari unsur yang terlibat dalam reaksi tersebut akan memiliki perbandingan tetap.
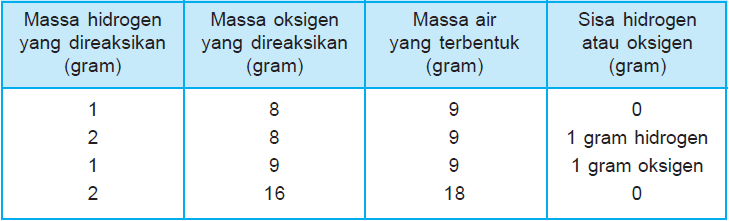
Hukum Perbandingan Tetap (Hukum Proust) | Plengdut.com
Hukum Perbandingan Tetap, juga dikenal sebagai Hukum Proust, adalah salah satu hukum dasar dalam kimia. Hukum ini menyatakan bahwa dalam suatu senyawa kimia, berat relatif setiap unsur akan selalu memiliki perbandingan tetap.

HUKUM PERBANDINGAN MASSA TETAP | HUKUM DASAR KIMIA | HUKUM PROUST – YouTube
Hukum Perbandingan Massa Tetap, yang juga dikenal sebagai Hukum Proust, merupakan salah satu konsep dasar dalam kimia. Hukum ini menyatakan bahwa ketika dua atau lebih zat bereaksi untuk membentuk zat lain, massa setiap zat yang terlibat dalam reaksi tersebut akan memiliki perbandingan tetap.
Apa itu Hukum Perbandingan Tetap atau Hukum Proust? Hukum Perbandingan Tetap atau Hukum Proust adalah prinsip dasar dalam kimia yang menyatakan bahwa ketika dua atau lebih unsur bereaksi untuk membentuk zat lain, massa setiap unsur yang terlibat dalam reaksi tersebut akan memiliki perbandingan tetap. Ini berarti bahwa setiap massa relatif dari unsur atau senyawa yang terlibat dalam reaksi kimia akan selalu berada dalam perbandingan yang tetap.
Siapa yang menemukan Hukum Perbandingan Tetap atau Hukum Proust? Hukum Perbandingan Tetap atau Hukum Proust pertama kali ditemukan oleh seorang ahli kimia bernama Joseph Louis Proust pada tahun 1794. Proust adalah seorang ilmuwan asal Prancis yang mengemukakan hukum ini setelah melakukan serangkaian percobaan dan observasi tentang reaksi kimia.
Kapan Hukum Perbandingan Tetap atau Hukum Proust ditemukan? Hukum Perbandingan Tetap atau Hukum Proust ditemukan pada tahun 1794 oleh Joseph Louis Proust. Pada saat itu, Proust sedang melakukan penelitian tentang reaksi kimia dan perbandingan massa yang terlibat dalam reaksi tersebut. Berkat penelitiannya tersebut, Proust berhasil menemukan hukum ini dan menjelaskan prinsip dasar di balik perbandingan tetap dalam reaksi kimia.
Dimana Hukum Perbandingan Tetap atau Hukum Proust ditemukan? Hukum Perbandingan Tetap atau Hukum Proust ditemukan oleh Joseph Louis Proust di Prancis. Proust melakukan serangkaian percobaan dan observasi di laboratoriumnya untuk memahami lebih dalam tentang perbandingan massa yang terlibat dalam reaksi kimia. Hasil dari penelitiannya tersebut kemudian dijelaskan dan dipublikasikan dalam makalah ilmiah yang menjelaskan Hukum Perbandingan Tetap atau Hukum Proust.
Bagaimana Hukum Perbandingan Tetap atau Hukum Proust bekerja? Hukum Perbandingan Tetap atau Hukum Proust bekerja berdasarkan prinsip bahwa setiap unsur atau senyawa memiliki berat relatif yang tetap saat bereaksi membentuk senyawa lain. Ini berarti bahwa setiap massa relatif dari unsur atau senyawa yang terlibat dalam reaksi kimia akan selalu memiliki perbandingan tetap. Misalnya, ketika hidrogen (H2) bereaksi dengan oksigen (O2) untuk membentuk air (H2O), massa hidrogen dan oksigen yang terlibat dalam reaksi ini akan selalu memiliki perbandingan tetap, yaitu 2:1.
Cara menggunakan Hukum Perbandingan Tetap atau Hukum Proust dalam perhitungan kimia? Untuk menggunakan Hukum Perbandingan Tetap atau Hukum Proust dalam perhitungan kimia, kita perlu mengidentifikasi unsur atau senyawa yang terlibat dalam reaksi dan menentukan massa relatif masing-masing unsur atau senyawa. Kemudian, kita dapat menghitung perbandingan massa antara unsur atau senyawa tersebut berdasarkan hukum ini. Misalnya, jika kita ingin menghitung perbandingan massa antara hidrogen (H2) dan oksigen (O2) dalam reaksi pembentukan air (H2O), kita dapat menggunakan hukum ini untuk mengetahui bahwa perbandingan massa hidrogen terhadap oksigen adalah 2:1.
Kesimpulan Hukum Perbandingan Tetap atau Hukum Proust adalah salah satu konsep dasar dalam kimia yang menyatakan bahwa ketika dua atau lebih unsur atau senyawa bereaksi untuk membentuk senyawa lain, massa relatif setiap unsur atau senyawa akan memiliki perbandingan tetap. Hukum ini pertama kali ditemukan oleh Joseph Louis Proust pada tahun 1794 dan memiliki banyak aplikasi dalam perhitungan kimia. Hukum Perbandingan Tetap atau Hukum Proust sangat penting karena memungkinkan kita untuk memahami dan memprediksi perubahan massa yang terjadi dalam reaksi kimia.


