Cara Menghitung Energi Ionisasi
Pada artikel kali ini, kita akan membahas cara menghitung energi ionisasi. Sebelum memulai, kita perlu memahami terlebih dahulu apa itu energi ionisasi. Energi ionisasi merupakan energi yang diperlukan untuk mengionisasi atau melepaskan satu elektron dari suatu atom netral.
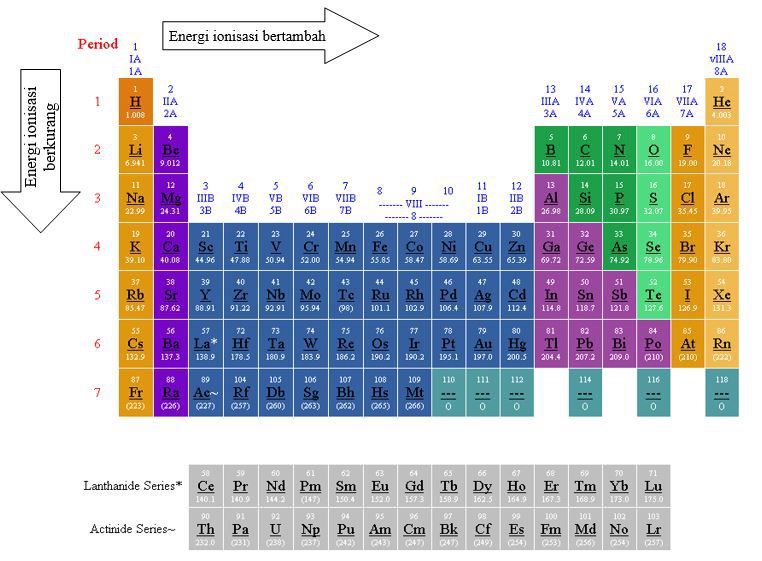
Apa itu Energi Ionisasi?
Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas. Setiap unsur memiliki energi ionisasi yang berbeda-beda, tergantung pada jumlah elektron yang harus dilepaskan dan struktur elektronnya.
Jari Jari Atom Unsur Dalam Satu Periode Dari Kiri Ke Kanan Semakin
Sekarang, mari kita bahas mengenai jari-jari atom unsur dalam satu periode dari kiri ke kanan. Jari-jari atom adalah jarak antara inti atom dengan elektron valensi terluar. Pada umumnya, jari-jari atom unsur dalam satu periode dari kiri ke kanan akan semakin mengecil.

Apa itu Jari-jari Atom Unsur?
Jari-jari atom unsur adalah jarak antara inti atom dengan elektron terluar. Jari-jari atom berkaitan dengan ukuran atom, yang berpengaruh pada sifat-sifat fisik dan kimia suatu unsur.
Materi – Sellyandika23
Dalam materi ini, Sellyandika23 membahas mengenai energi ionisasi. Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas.

Apa itu Energi Ionisasi?
Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas. Energi ionisasi dapat dihitung menggunakan persamaan berikut:
Energi Ionisasi = Energi Total Atom yang Dihidupkan – Energi Total Atom yang Dinyalakan Kembali
Jadi, energi ionisasi dapat dihitung dengan mengurangi energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan.
Cara Menghitung Energi Ionisasi
Berikut adalah langkah-langkah yang dapat dilakukan untuk menghitung energi ionisasi suatu atom:
- Tentukan energi total atom yang dinyalakan kembali setelah satu elektron dilepaskan.
- Tentukan energi total atom yang dihidupkan sebelum satu elektron dilepaskan.
- Kurangkan energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan untuk mendapatkan energi ionisasi.
Contoh perhitungan energi ionisasi:
Misalkan energi total atom yang dinyalakan kembali adalah 500 kJ/mol, dan energi total atom yang dihidupkan adalah 1000 kJ/mol.
Maka, energi ionisasi dapat dihitung sebagai berikut:
Energi Ionisasi = 1000 kJ/mol – 500 kJ/mol = 500 kJ/mol
Jadi, energi ionisasi atom tersebut adalah 500 kJ/mol.
Jari-jari Atom Unsur Dalam Satu Periode Dari Kiri Ke Kanan Semakin
Sebagai tambahan informasi, jari-jari atom unsur dalam satu periode dari kiri ke kanan akan semakin mengecil. Hal ini disebabkan oleh peningkatan jumlah proton dalam inti atom.

Apa itu Jari-jari Atom Unsur?
Jari-jari atom unsur adalah jarak antara inti atom dengan elektron terluar. Pada umumnya, jari-jari atom mengalami penurunan dari kiri ke kanan dalam satu periode dikarenakan peningkatan jumlah proton dalam inti atom.
Materi – Sellyandika23
Materi ini dibuat oleh Sellyandika23 dan berisi informasi mengenai energi ionisasi. Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas.

Apa itu Energi Ionisasi?
Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas. Energi ionisasi dapat dihitung menggunakan persamaan berikut:
Energi Ionisasi = Energi Total Atom yang Dihidupkan – Energi Total Atom yang Dinyalakan Kembali
Jadi, energi ionisasi dapat dihitung dengan mengurangi energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan.
Cara Menghitung Energi Ionisasi
Berikut adalah langkah-langkah yang dapat dilakukan untuk menghitung energi ionisasi suatu atom:
- Tentukan energi total atom yang dinyalakan kembali setelah satu elektron dilepaskan.
- Tentukan energi total atom yang dihidupkan sebelum satu elektron dilepaskan.
- Kurangkan energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan untuk mendapatkan energi ionisasi.
Contoh perhitungan energi ionisasi:
Misalkan energi total atom yang dinyalakan kembali adalah 500 kJ/mol, dan energi total atom yang dihidupkan adalah 1000 kJ/mol.
Maka, energi ionisasi dapat dihitung sebagai berikut:
Energi Ionisasi = 1000 kJ/mol – 500 kJ/mol = 500 kJ/mol
Jadi, energi ionisasi atom tersebut adalah 500 kJ/mol.
Jari-jari Atom Unsur Dalam Satu Periode Dari Kiri Ke Kanan Semakin
Sebagai tambahan informasi, jari-jari atom unsur dalam satu periode dari kiri ke kanan akan semakin mengecil. Hal ini disebabkan oleh peningkatan jumlah proton dalam inti atom.

Apa itu Jari-jari Atom Unsur?
Jari-jari atom unsur adalah jarak antara inti atom dengan elektron terluar. Pada umumnya, jari-jari atom mengalami penurunan dari kiri ke kanan dalam satu periode dikarenakan peningkatan jumlah proton dalam inti atom.
Materi – Sellyandika23
Materi ini dibuat oleh Sellyandika23 dan berisi informasi mengenai energi ionisasi. Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas.

Apa itu Energi Ionisasi?
Energi ionisasi adalah energi minimum yang diperlukan untuk melepaskan satu elektron dari suatu unsur dalam keadaan gas. Energi ionisasi dapat dihitung menggunakan persamaan berikut:
Energi Ionisasi = Energi Total Atom yang Dihidupkan – Energi Total Atom yang Dinyalakan Kembali
Jadi, energi ionisasi dapat dihitung dengan mengurangi energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan.
Cara Menghitung Energi Ionisasi
Berikut adalah langkah-langkah yang dapat dilakukan untuk menghitung energi ionisasi suatu atom:
- Tentukan energi total atom yang dinyalakan kembali setelah satu elektron dilepaskan.
- Tentukan energi total atom yang dihidupkan sebelum satu elektron dilepaskan.
- Kurangkan energi total atom yang dinyalakan kembali dengan energi total atom yang dihidupkan untuk mendapatkan energi ionisasi.
Contoh perhitungan energi ionisasi:
Misalkan energi total atom yang dinyalakan kembali adalah 500 kJ/mol, dan energi total atom yang dihidupkan adalah 1000 kJ/mol.
Maka, energi ionisasi dapat dihitung sebagai berikut:
Energi Ionisasi = 1000 kJ/mol – 500 kJ/mol = 500 kJ/mol
Jadi, energi ionisasi atom tersebut adalah 500 kJ/mol.
Jari-jari Atom Unsur Dalam Satu Periode Dari Kiri Ke Kanan Semakin
Sebagai tambahan informasi, jari-jari atom unsur dalam satu periode dari kiri ke kanan akan semakin mengecil. Hal ini disebabkan oleh peningkatan jumlah proton dalam inti atom.

Apa itu Jari-jari Atom Unsur?
Jari-jari atom unsur adalah jarak antara inti atom dengan elektron terluar. Pada umumnya, jari-jari atom mengalami penurunan dari kiri ke kanan dalam satu periode dikarenakan peningkatan jumlah proton dalam inti atom.


