Reaksi redoks atau reaksi reduksi dan oksidasi adalah salah satu jenis reaksi kimia yang sering ditemui dalam kehidupan sehari-hari. Reaksi redoks terjadi ketika terdapat perubahan pada bilangan oksidasi atom dalam suatu senyawa atau molekul. Untuk dapat memahami lebih dalam mengenai reaksi redoks, mari kita bahas lebih lanjut dengan pembahasan berikut ini.
Apa Itu Reaksi Redoks?
Reaksi redoks adalah reaksi kimia yang terjadi karena adanya perubahan bilangan oksidasi pada suatu senyawa atau molekul. Reaksi ini terdiri dari dua bagian, yaitu reaksi reduksi dan reaksi oksidasi. Reaksi reduksi (red) terjadi ketika terdapat penambahan elektron pada suatu senyawa atau molekul, sedangkan reaksi oksidasi (oks) terjadi ketika terdapat pengurangan elektron pada suatu senyawa atau molekul.
Mengapa Reaksi Redoks Penting?
Reaksi redoks memiliki banyak kegunaan dalam kehidupan sehari-hari, seperti dalam produksi energi, pengolahan logam, pembusukan bahan makanan, dan masih banyak lagi. Dalam produksi energi, contohnya, reaksi redoks digunakan dalam baterai dan sel bahan bakar. Sedangkan dalam pengolahan logam, reaksi redoks digunakan untuk memurnikan logam dari mineral.
Cara Menyelesaikan Persamaan Reaksi Redoks
Untuk menyelesaikan persamaan reaksi redoks, pertama-tama kita harus menentukan senyawa apa saja yang mengalami reaksi redoks. Kemudian, kita harus menentukan bilangan oksidasi setiap unsur dalam senyawa tersebut sebelum dan sesudah reaksi berlangsung. Setelah itu, kita dapat menyusun persamaan reaksi dengan memperhatikan bahwa reaksi reduksi harus seimbang dengan reaksi oksidasi.
Contoh Soal Reaksi Redoks
Berikut adalah contoh soal reaksi redoks beserta pembahasannya:
Soal
Sebuah larutan seng sulfat (ZnSO4) dilarutkan dengan elektroda permukaan Pt. Elektroda dikalibrasi dengan elektroda hidrogen (Eh = 0 V) dan elektroda seng/seng sulfat (EZn = -0.76 V). Hitung potensial sel dan tuliskan persamaan reaksi redoks yang terjadi.
Pembahasan
Pertama, kita harus menentukan senyawa apa saja yang terlibat dalam reaksi redoks. Dalam soal ini, senyawa yang terlibat adalah seng sulfat (ZnSO4). Selanjutnya, kita harus menentukan bilangan oksidasi setiap unsur dalam senyawa tersebut sebelum dan sesudah reaksi berlangsung.
- Zn: +2 (sebelum) → 0 (setelah)
- S: +6 (sebelum) → +6 (setelah)
- O: -2 (sebelum) → -2 (setelah)
Setelah menentukan bilangan oksidasi, kita dapat menyusun persamaan reaksi. Dalam reaksi ini, elektroda Pt bertindak sebagai elektroda reduksi dan seng sulfat bertindak sebagai elektroda oksidasi.
Elektroda reduksi:
Zn2+(aq) + 2e– → Zn(s) (EZn = -0.76 V)
Elektroda oksidasi:
SO42-(aq) → 2e– + 1/2O2(g) + 2H+(aq)
Jika kita menambahkan kedua persamaan reaksi tersebut, kita akan mendapatkan persamaan reaksi redoks:
ZnSO4(aq) + O2(g) + 2H+ → Zn(s) + SO42-(aq) + H2O(l)
Untuk menghitung potensial sel, kita dapat menggunakan persamaan:
Esel = Ered – Eoks
Sehingga,
Esel = EZn – (0.0592/2) log([Zn2+]/[SO42-][H+]2) – 0.64
Dalam soal ini, [Zn2+] = 1 M, [SO42-] = 1 M, dan [H+] = 1 M. Sehingga,
Esel = -0.76 – 0 – 0.64
Esel = -1.4 V
Jadi, potensial sel dalam reaksi redoks ini adalah -1.4 V.
Dengan memahami reaksi redoks, kita dapat memahami lebih dalam mengenai berbagai proses kimia yang terjadi dalam kehidupan sehari-hari. Selain itu, dengan menguasai teknik menyelesaikan persamaan reaksi redoks, kita dapat menyelesaikan berbagai permasalahan yang berkaitan dengan reaksi kimia dalam kehidupan sehari-hari.

Contoh Soal Essay Reaksi Redoks
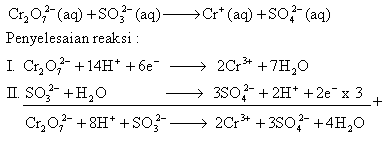
1. Jelaskan apa yang dimaksud dengan reaksi redoks!
2. Sebutkan contoh reaksi redoks yang terjadi dalam kehidupan sehari-hari!
3. Jelaskan cara menyelesaikan persamaan reaksi redoks!
4. Berikan contoh soal mengenai reaksi redoks beserta pembahasannya!
Jawaban:
1. Reaksi redoks adalah reaksi kimia yang terjadi karena adanya perubahan bilangan oksidasi pada suatu senyawa atau molekul.
2. Contoh reaksi redoks yang terjadi dalam kehidupan sehari-hari antara lain adalah pembusukan bahan makanan, produksi energi dalam baterai, dan pengolahan logam.
3. Untuk menyelesaikan persamaan reaksi redoks, pertama-tama kita harus menentukan senyawa apa saja yang mengalami reaksi redoks. Selanjutnya, kita harus menentukan bilangan oksidasi setiap unsur dalam senyawa tersebut sebelum dan sesudah reaksi berlangsung. Setelah itu, kita dapat menyusun persamaan reaksi dengan memperhatikan bahwa reaksi reduksi harus seimbang dengan reaksi oksidasi.
4. Sebuah larutan seng sulfat (ZnSO4) dilarutkan dengan elektroda permukaan Pt. Elektroda dikalibrasi dengan elektroda hidrogen (Eh = 0 V) dan elektroda seng/seng sulfat (EZn = -0.76 V). Hitung potensial sel dan tuliskan persamaan reaksi redoks yang terjadi.
Pertama, kita harus menentukan senyawa apa saja yang terlibat dalam reaksi redoks. Dalam soal ini, senyawa yang terlibat adalah seng sulfat (ZnSO4). Selanjutnya, kita harus menentukan bilangan oksidasi setiap unsur dalam senyawa tersebut sebelum dan sesudah reaksi berlangsung.
- Zn: +2 (sebelum) → 0 (setelah)
- S: +6 (sebelum) → +6 (setelah)
- O: -2 (sebelum) → -2 (setelah)
Setelah menentukan bilangan oksidasi, kita dapat menyusun persamaan reaksi. Dalam reaksi ini, elektroda Pt bertindak sebagai elektroda reduksi dan seng sulfat bertindak sebagai elektroda oksidasi.
Elektroda reduksi:
Zn2+(aq) + 2e– → Zn(s) (EZn = -0.76 V)
Elektroda oksidasi:
SO42-(aq) → 2e– + 1/2O2(g) + 2H+(aq)
Jika kita menambahkan kedua persamaan reaksi tersebut, kita akan mendapatkan persamaan reaksi redoks:
ZnSO4(aq) + O2(g) + 2H+ → Zn(s) + SO42-(aq) + H2O(l)
Untuk menghitung potensial sel, kita dapat menggunakan persamaan:
Esel = Ered – Eoks
Sehingga,
Esel = EZn – (0.0592/2) log([Zn2+]/[SO42-][H+]2) – 0.64
Dalam soal ini, [Zn2+] = 1 M, [SO42-] = 1 M, dan [H+] = 1 M. Sehingga,
Esel = -0.76 – 0 – 0.64
Esel = -1.4 V
Jadi, potensial sel dalam reaksi redoks ini adalah -1.4 V.